Lungenfibrose: Mehr Atemzüge dank früher antifibrotischer ILD-Therapie
Haben Sie ein standardisiertes Vorgehen für den Beginn einer antifibrotischen Therapie bei Lungenfibrose? Die Zeit läuft, denn verlorene Lungenfunktion ist unwiederbringlich. Und je höher der FVC-Verlust, desto höher ist auch das Risiko für akute ILD-Exazerbationen und Tod – schnelles Handeln ist also gefragt.1,2 Um die Prognose der Betroffenen zu verbessern*, ist ein frühzeitiger Therapiebeginn essenziell.
Fünf Gründe, warum die Therapie der Lungenfibrose zeitkritisch ist
1. IPF ist tödlicher als viele Krebsarten
Mit einer medianen Überlebenszeit von 2–3 Jahren und einer 5-Jahres-Überlebensrate von etwa 20–40 % weist eine unbehandelte idiopathische Lungenfibrose (IPF) eine niedrigere 5-Jahres-Überlebensrate auf als die meisten Tumorentitäten.3 Tatsächlich haben nur das Pankreas- und Lungen-Karzinom eine schlechtere Überlebensrate als die IPF.
Bei einem Krebs-Verdacht wird zurecht höchste Priorität an den Tag gelegt. Sollte die Lungenfibrose konsequenterweise dann nicht auch eine ähnliche Priorität erfahren?
2. Lungenfunktion: Was weg ist, ist weg
Der Verlauf einer progredienten pulmonalen Fibrose (PPF)** ist meist nicht vorhersehbar und individuell sehr unterschiedlich. Fest steht jedoch: die krankheitsbedingten Veränderungen im Lungengewebe sind irreversibel und gehen mit einem zunehmenden Verlust der Lungenfunktion einher.4 Die Folgen für betroffene Patient:innen sind fatal: Zunehmende Atemnot und Husten schränken Alltagsaktivitäten und die Lebensqualität erheblich ein.5, 6, 7 ,8 Zudem sinkt mit zunehmendem Verlust der Lungenfunktion die Überlebenswahrscheinlichkeit enorm und das Risiko für akute Exazerbationen steigt.1, 2
3. Akute ILD-Exazerbationen: plötzlich, unvorhersehbar und dramatisch für Verlauf und Prognose

Akute Exazerbationen stellen für betroffene Patient:innen oftmals einen Wendepunkt im Verlauf der Erkrankung dar und gelten als DIE wesentliche Komplikation einer Lungenfibrose.9 Denn wenn sie auftreten, sind sie meist verheerend: Nahezu 50 % der IPF-Patient:innen versterben infolge dieser akuten Verschlechterung, die mediane Überlebensdauer beträgt etwa 3 bis 4 Monate.9 Aber nicht nur IPF-Patient:innen sind gefährdet, akute Exazerbationen können bei allen PPFs jederzeit spontan auftreten, wobei die Prognose immer schlecht ist.2 Sie zu vermeiden ist darum ein wichtiges therapeutisches Ziel.
4. Leitlinien empfehlen antifibrotische Therapie bei Lungenfibrose

Eine antifibrotische Therapie kann die Chancen von Patient:innen mit idiopathischer Lungenfibrose (IPF) und anderen progredienten Lungenfibrosen (PPF) verbessern und wird in nationalen und internationalen Leitlinien empfohlen.10, 11, 12, 13 Sie handeln leitlinienkonform, wenn Sie
- eine IPF ab Diagnose sowie alle andere progredienten pulmonalen Fibrosen (z.B. fibrotische EAA) antifibrotisch therapieren.10, 11, 12
- eine antifibrotische Therapie bei SSc-ILD ab Diagnosestellung einleiten. Ein zuvor erbrachter Progredienznachweis ist nicht erforderlich.13
Dennoch offenbaren aktuelle Umfrageergebnisse unter Pneumolog:innen, dass sich dies noch nicht flächendeckend in der täglichen Praxis widerspiegelt.14
5. Fibrose braucht Antifibrose
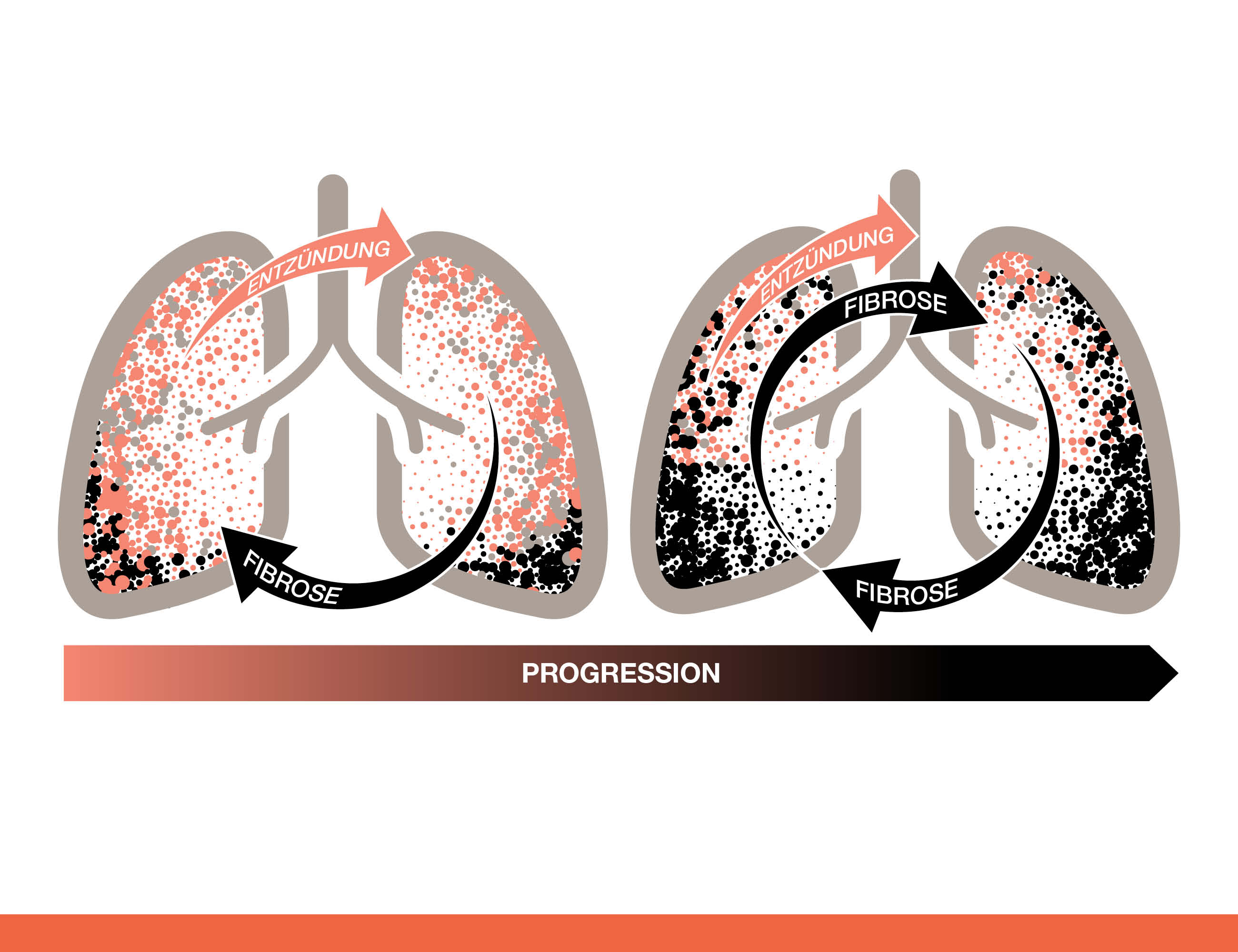
Immunmodulatorische Therapien spielen eine tragende Rolle in der Behandlung vieler Autoimmunerkrankungen (z. B. rheumatoide Arthritis, systemische Sklerose), haben jedoch keinen direkten antifibrotischen Effekt, der die selbsterhaltenden Mechanismen der Fibrose unterbindet.15, 16, 17, 18 Dabei ist die Lungenfibrose eine der Haupttodesursachen bei vielen AI-ILDs.19, 20 Da bei einer ILD sowohl entzündliche als auch fibrotische Prozesse eine Rolle spielen können, ist es wichtig, sowohl die Entzündung als auch die Fibrose gezielt zu therapieren, um die Lungenfunktion möglichst lange zu erhalten.
Ein frühzeitiger und konsequenter Therapiebeginn erhöht die Chance, den Krankheitsverlauf Ihrer Lungenfibrose-Patient:innen positiv zu beeinflussen und die Lebensqualität länger zu erhalten.
Worauf warten Sie noch?
Für medizinische Fachkreise gibt es mehr Informationen zu den Vorteilen einer antifibrotischen Therapie inkl. Studiendaten nach Login.
Exklusiv für Fachkreise und Behandlungsteams
Jetzt kostenfrei anmelden oder registrieren und uneingeschränkten Zugriff auf unsere Services
erhalten
Sie haben Symptome? Machen Sie jetzt den Lungenfibrose-Selbsttest
Anhaltender trockener Husten, Atemnot, Müdigkeit? Diese Symptome können viele Ursachen haben, doch manchmal kann eine Lungenfibrose dahinterstecken. Unser kurzer Selbsttest hilft Ihnen, erste Anhaltspunkte zu finden und zu entscheiden, ob ein Arztbesuch sinnvoll ist. Der Test dauert nur ca. 3 Minuten und Ihre eingegebenen Daten bleiben dabei anonym.
Ihre Gesundheit zählt!
Sie sind von der Diagnose Lungenfibrose betroffen? Unterstützung für den Alltag mit der Erkrankung
Unsere unten aufgeführten Internetseiten bieten Ihnen verlässliche und gut verständliche Informationen rund um die Erkrankung.
Dort finden Sie Wissenswertes über die Ursachen und Symptome, über Untersuchungsmethoden und Behandlungsmöglichkeiten bei Lungenfibrose. Außerdem erhalten Sie praktische Tipps, wie Sie Ihren Alltag mit der Erkrankung besser bewältigen können. Mit Broschüren zu den Krankheitsbildern sowie hilfreichen Ratgebern, Postern und Dokumentationshilfen rund um die Themen Ernährung und Bewegung können Sie darüber hinaus zahlreiche Materialien direkt herunterladen oder bestellen.
Jetzt Informationsvorteil sichern!
Fußnoten
- * Gemessen am FVC-Verlust.
- ** Die Bezeichnung PPF wird in nationalen und internationalen Leitlinien benutzt und ist synonym mit der bisherigen Bezeichnung PF-ILD zu verstehen10,12 die im Zulassungstext der EMA verwendet wird.
Referenzen
- 1 Maher TM et al., Respirology. 2023;10.1111/resp.14579.
- 2 Alhamad EH, et al. Ann Thorac Med. 2021;16(2):178–187.
- 3 Vancheri C et al. Eur Respir J. 2010;35:496–504.
- 4 Richeldi L et al., Lancet. 2017;389(10082):1941-52.
- 5 Wuyts WA et al., Adv Ther. 2020;37(7):3246–64.
- 6 Swigris JJ et al., Eur Respir Rev. 2018;27(150):pii:180075.
- 7 Morisset J et al.; Ann Am Thorac Soc. 2016;13:1026–33.
- 8 Olson AL, Brown KK, Swigris JJ, Patient Relat Outcome Meas. 2016;7:29–35.
- 9 Collard HR et al., Am J Respir Crit Care Med. 2016;194(3):265-75.
- 10 Behr J et al., Pneumologie 2023;77(02):94–119.
- 11 Koschel D et al., Pneumologie 2024;78(12):963–1002.
- 12 Raghu G et al., Am J Respir Crit Care Med. 2022;205(9):e18–e47.
- 13 Del Galdo F et al., Ann Rheum Dis. 2024;17:ard-2024–226430.
- 14 Data on file, Boehringer Ingelheim.
- 15 Flaherty KR et al., BMJ Open Resp Res. 2017;4(1):e000212.
- 16 Patterson KC und Strek ME. Ann Am Thorac Soc. 2013;10(4):362–70.
- 17 Caban JJ et al., Conf Proc IEEE Eng Med Biol Soc. 2011;2011:6216–19.
- 18 Wells AU et al., Eur Respir J. 2018;51(5):1800692.
- 19 Ewig S, Bollow M. Z Rheumatol. 2021;80(1):S13–S32.
- 20 Steen, V. D. & Medsger, T. A. Ann. Rheum. Dis. 2007;66:940–944.
![[site:name]](/de/sites/default/files/2022-11/bi-logo.png)